Page 16 - VISION 1 Real World Data
P. 16
FORSCHUNG UND WISSENSCHAFT
Behandlungsrealität von Patienten mit mCRC nach
ihrem KRAS- bzw. RAS-Mutationsstatus
Mit der Entwicklung der monoklonalen Antikörper zur EGFR-
Inhibition wurde auch die (K)RAS-Testung eingeführt. Wie hat
sich die Testung etabliert? Welche Veränderungen brachte das für
die Behandlung? Wie ist das Gesamtüberleben von Patienten mit Kolorektalkarzinom
mCRC mit bzw. ohne RAS-Mutation im Behandlungsalltag?
Bereits 2004 wurde Cetuximab als Durch die Testung auf ein breiteres
erster monoklonaler Antikörper zur Spektrum an Mutationen veränderte
Behandlung von Patienten mit metas- sich das Verhältnis von Patienten mit
tasiertem kolorektalen Karzinom einem Wildtyp-Tumor zu Patienten mit
(mCRC) zugelassen. Panitumumab einem Tumor mit Mutation: Während
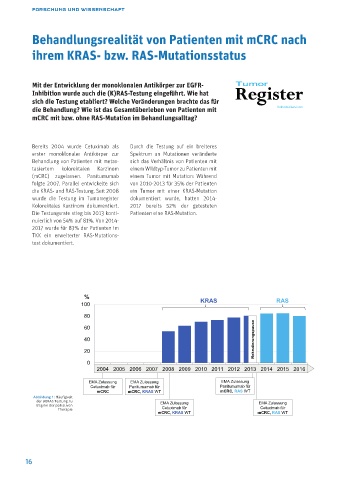
folgte 2007. Parallel entwickelte sich von 2010-2013 für 35% der Patienten
die KRAS- und RAS-Testung. Seit 2008 ein Tumor mit einer KRAS-Mutation
wurde die Testung im Tumorregister dokumentiert wurde, hatten 2014-
Kolorektales Karzinom dokumentiert. 2017 bereits 52% der getesteten
Die Testungsrate stieg bis 2013 konti- Patienten eine RAS-Mutation.
nuierlich von 54% auf 81%. Von 2014-
2017 wurde für 83% der Patienten im
TKK ein erweiterter RAS-Mutations-
test dokumentiert.
%
100 KRAS RAS
80
Rekrutierungspause
60
40
20
0
2004 2005 2006 2007 2008 2009 2010 2011 2012 2013 2014 2015 2016
EMA Zulassung EMA Zulassung EMA Zulassung
Cetuximab für Panitumumab für Panitumumab für
mCRC mCRC, KRAS WT mCRC, RAS WT
Abbildung 1: Häufigkeit
der (K)RAS Testung zu EMA Zulassung EMA Zulassung
Beginn der palliativen
Therapie Cetuximab für Cetuximab für
mCRC, KRAS WT mCRC, RAS WT
16